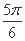
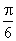 个单位,再把纵坐标伸长到原来的3倍(横坐标不变) 把图像上所有点向左平行移动
个单位,再把纵坐标伸长到原来的3倍(横坐标不变) 把图像上所有点向左平行移动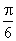 个单位,再把纵坐标伸长到原来的3倍(横坐标不变) 把图像上所有点向右平行移动
个单位,再把纵坐标伸长到原来的3倍(横坐标不变) 把图像上所有点向右平行移动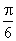 个单位,再把纵坐标缩短到原来的
个单位,再把纵坐标缩短到原来的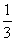 倍(横坐标不变) 把图像上所有点向左平行移动
倍(横坐标不变) 把图像上所有点向左平行移动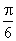 个单位,再把纵坐标缩短到原来的
个单位,再把纵坐标缩短到原来的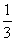 倍(横坐标不变)
倍(横坐标不变)
 倍(纵坐标不变),再向右平移
倍(纵坐标不变),再向右平移 个单位长度 横坐标缩短到原来的
个单位长度 横坐标缩短到原来的 倍(纵坐标不变),再向右平移
倍(纵坐标不变),再向右平移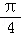 个单位长度 横坐标缩短到原来的2倍(纵坐标不变),再向右平移
个单位长度 横坐标缩短到原来的2倍(纵坐标不变),再向右平移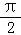 个单位长度 横坐标缩短到原来的2倍(纵坐标不变),再向右平移
个单位长度 横坐标缩短到原来的2倍(纵坐标不变),再向右平移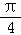 个单位长度
个单位长度
 ,x∈R y=sin2x,x∈R y=
,x∈R y=sin2x,x∈R y= sinx,x∈R y=2sinx,x∈R.
sinx,x∈R y=2sinx,x∈R.
 倍,再向右平移
倍,再向右平移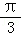 个单位长度 横坐标伸长到原来的
个单位长度 横坐标伸长到原来的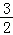 倍,再向右平移
倍,再向右平移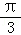 个单位长度 横坐标缩短到原来的
个单位长度 横坐标缩短到原来的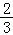 倍,再向左平移
倍,再向左平移 个单位长度 横坐标伸长到原来的
个单位长度 横坐标伸长到原来的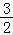 倍,再向左平移
倍,再向左平移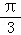 个单位长度
个单位长度
 倍,纵坐标不变 纵坐标缩短到原来的
倍,纵坐标不变 纵坐标缩短到原来的 倍,横坐标不变
倍,横坐标不变
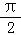 )在定义域内的图象,为了得到该函数的图象,只需将函数y=sinx的图象上所有点( )
)在定义域内的图象,为了得到该函数的图象,只需将函数y=sinx的图象上所有点( )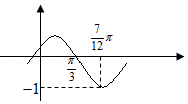
A.向左平移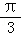 个单位长度,再把所得图象各点的横坐标缩短到原来的
个单位长度,再把所得图象各点的横坐标缩短到原来的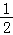 ,纵坐标不变
,纵坐标不变
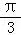 个单位长度,再把所得图象各点的横坐标缩短到原来的
个单位长度,再把所得图象各点的横坐标缩短到原来的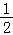 ,纵坐标不变 向左平移
,纵坐标不变 向左平移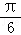 个单位长度,再把所得图象各点的横坐标缩短到原来的
个单位长度,再把所得图象各点的横坐标缩短到原来的 ,纵坐标不变 向左平移
,纵坐标不变 向左平移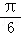 个单位长度,再把所得图象各点的横坐标伸长到原来的2倍,纵坐标不变
个单位长度,再把所得图象各点的横坐标伸长到原来的2倍,纵坐标不变
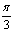 个单位,再把所有点的横坐标伸长到原来的2倍,纵坐标不变 向右平移
个单位,再把所有点的横坐标伸长到原来的2倍,纵坐标不变 向右平移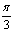 个单位,再把所有点的横坐标伸长到原来的2倍,纵坐标不变 向左平移
个单位,再把所有点的横坐标伸长到原来的2倍,纵坐标不变 向左平移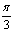 个单位,再把所有点的横坐书缩短到原来的
个单位,再把所有点的横坐书缩短到原来的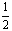 倍,纵坐标不变 向右平移
倍,纵坐标不变 向右平移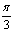 个单位,再把所有点的横坐标缩短到原来的
个单位,再把所有点的横坐标缩短到原来的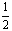 倍,纵坐标不变
倍,纵坐标不变
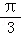 个单位,再将所得图象上所有点的纵坐标伸长到原来的2倍,横坐标不变得到 向右平移
个单位,再将所得图象上所有点的纵坐标伸长到原来的2倍,横坐标不变得到 向右平移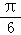 个单位,再将所得图象上所有点的纵坐标伸长到原来的2倍,横坐标不变得到 向左平移
个单位,再将所得图象上所有点的纵坐标伸长到原来的2倍,横坐标不变得到 向左平移 个单位,再将所得图象上所有点的纵坐标缩短到原来的
个单位,再将所得图象上所有点的纵坐标缩短到原来的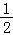 横坐标不变得到 向左平移
横坐标不变得到 向左平移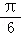 个单位,再将所得图象上所有点的纵坐标缩短到原来的
个单位,再将所得图象上所有点的纵坐标缩短到原来的 横坐标不变得到
横坐标不变得到
 倍,横坐标不变,再向右平移1个单位长度 纵坐标缩短到原来的
倍,横坐标不变,再向右平移1个单位长度 纵坐标缩短到原来的 倍,横坐标不变,再向左平移1个单位长度 横坐标伸长到原来的2倍,纵坐标不变,再向左平移1个单位长度 横坐标伸长到原来的2倍,纵坐标不变,再向右平移1个单位长度
倍,横坐标不变,再向左平移1个单位长度 横坐标伸长到原来的2倍,纵坐标不变,再向左平移1个单位长度 横坐标伸长到原来的2倍,纵坐标不变,再向右平移1个单位长度
 倍,纵坐标不变 纵坐标伸长到原来的4倍,横坐标不变 纵坐标缩短到原来的
倍,纵坐标不变 纵坐标伸长到原来的4倍,横坐标不变 纵坐标缩短到原来的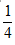 倍,横坐标不变
倍,横坐标不变
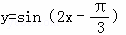 ,x∈R
,x∈R 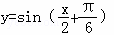 ,x∈R
,x∈R 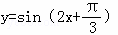 ,x∈R
,x∈R 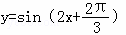 ,x∈R
,x∈R
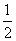 ,横坐标不变,再向右平移1个单位 纵坐标缩短到原来的
,横坐标不变,再向右平移1个单位 纵坐标缩短到原来的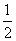 ,横坐标不变,再向左平移1个单位 横坐标伸长到原来的2倍,纵坐标不变,再向左平移1个单位 横坐标伸长到原来的2倍,纵坐标不变,再向右平移1个单位
,横坐标不变,再向左平移1个单位 横坐标伸长到原来的2倍,纵坐标不变,再向左平移1个单位 横坐标伸长到原来的2倍,纵坐标不变,再向右平移1个单位
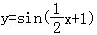
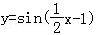
 个单位,再把横坐标伸长到原来的3倍(纵坐标不变) 把图象上所有点向左平行移动
个单位,再把横坐标伸长到原来的3倍(纵坐标不变) 把图象上所有点向左平行移动 个单位,再把横坐标伸长到原来的
个单位,再把横坐标伸长到原来的 倍(纵坐标不变) 把图象上所有点向右平行移动
倍(纵坐标不变) 把图象上所有点向右平行移动 个单位,再把横坐标缩短到原来的3倍(纵坐标不变) 把图象上所有点向右平行移动
个单位,再把横坐标缩短到原来的3倍(纵坐标不变) 把图象上所有点向右平行移动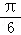 个单位,再把横坐标缩短到原来的
个单位,再把横坐标缩短到原来的 倍(纵坐标不变)
倍(纵坐标不变)
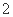 倍,横坐标向左平移
倍,横坐标向左平移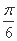 纵坐标缩短到原来的
纵坐标缩短到原来的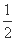 倍,横坐标向左平移
倍,横坐标向左平移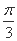 纵坐标伸长到原来的
纵坐标伸长到原来的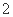 倍,横坐标向左平移
倍,横坐标向左平移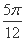 纵坐标缩短到原来的
纵坐标缩短到原来的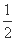 倍,横坐标向左平移
倍,横坐标向左平移