你可能感兴趣的试题
CO2+2H2O→CH4+2O2 NaOH+HCl = NaCl+H2O Cu+2HCl = Cu Cl2+H2↑ 4Al+3O2+6H2O = 4Al(OH)3
H2O、CH3COOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 H2SO4、NaOH . NaCl均为强电解质,都属于离子化合物 Al、Al2O3、Al(OH)3均既能与盐酸反应又能与氢氧化钠反应,都属于两性化合物 溶液、胶体、浊液均为分散系,都属于混合物
铝是还原剂,其还原产物是Al(OH)3 NaOH是氧化剂,其还原产物是H2 铝是还原剂,H2O和NaOH都是氧化剂 H2O是氧化剂,Al被氧化
盐酸与NaOH溶液的反应 H + H= H2 Al和Fe2O3的铝热反应 Ba(OH)2.8H2O与NH4Cl反应
2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑ 2Na + 2H2O =2NaOH + H2↑ 2F2 + 2H2O = 4HF + O2 Na2O + 2H2O = 2NaOH
H2O、CH3COOH、Cu2(OH)2CO3均含有氧元素,都是氧化物 H2SO4、NaOH、NaC1均为强电解质,都属于离子化合物 Al、Al2O3、Al(OH)3均能与盐酸反应又能与氢氧化钠溶液反应,都是具两性的化合物 溶液、胶体、浊液均为分散系,都属于混合物
2 H2O2  2 H2O + O2↑ 2 Al(OH)3
2 H2O + O2↑ 2 Al(OH)3  Al2O3 + 3 H2O FeO + 2 HCl = FeCl2 + H2O CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl
Al2O3 + 3 H2O FeO + 2 HCl = FeCl2 + H2O CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl
常见的酸溶液:H.2O.、HCl 、H.2SO4 常见的黑色固体:Mg、MnO2、Fe3O.4 常见的有还原性的物质:C.CO 、O.2 常见的碱性溶液:KOH溶液、Na2CO3溶液、NaOH溶液
(1)属于复分解反应 (2)属于放热反应 (3)属于中和反应 (4)属于分解反应
金属Fe与稀H2SO4反应:Fe + 2H+ == Fe3+ + H2↑ Al(OH)3治疗胃酸过多:H.++OH—===H2O NaHCO3溶液与NaOH溶液混合:HCO3—+OH— ==H2O + CO2↑ Al与NaOH溶液反应:2Al+2OH-+2H2O===2AlO +3H2↑
+3H2↑
铝粉投入到NaOH溶液中2Al+2OH-====2 +2H2O Al(OH)3溶于NaOH溶液Al(OH)3+OH-====
+2H2O Al(OH)3溶于NaOH溶液Al(OH)3+OH-==== +2H2O Al(OH)3溶于HCl溶液Al(OH)3+3H+====Al3++3H2O Al2O3粉末溶于NaOH溶液Al2O3+2OH-====2
+2H2O Al(OH)3溶于HCl溶液Al(OH)3+3H+====Al3++3H2O Al2O3粉末溶于NaOH溶液Al2O3+2OH-====2 +H2O
+H2O
氧化剂是NaOH 反应中的Al被还原 生成3mol H2时转移了6mol电子 1molAl失电子,有2molH2O中的氢得电子
Al(OH)3与盐酸反应: Al(OH)3+3H+===Al3++3H2O Al2O3溶于过量NaOH溶液: Al2O3+2OH-===2AlO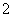 +H2O 铁溶于稀H2SO4∶Fe+2H+===Fe2++H2↑ Al(OH)3溶于NaOH溶液: Al(OH)3+3OH-===AlO
+H2O 铁溶于稀H2SO4∶Fe+2H+===Fe2++H2↑ Al(OH)3溶于NaOH溶液: Al(OH)3+3OH-===AlO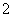 +3H2O
+3H2O

 2 H2O + O2↑ 2 Al(OH)3
2 H2O + O2↑ 2 Al(OH)3  Al2O3 + 3 H2O FeO + 2 HCl = FeCl2 + H2O CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl
Al2O3 + 3 H2O FeO + 2 HCl = FeCl2 + H2O CuCl2 + 2 NaOH = Cu(OH)2↓+ 2NaCl
 +3H2↑
+3H2↑
 +2H2O Al(OH)3溶于NaOH溶液Al(OH)3+OH-====
+2H2O Al(OH)3溶于NaOH溶液Al(OH)3+OH-==== +2H2O Al(OH)3溶于HCl溶液Al(OH)3+3H+====Al3++3H2O Al2O3粉末溶于NaOH溶液Al2O3+2OH-====2
+2H2O Al(OH)3溶于HCl溶液Al(OH)3+3H+====Al3++3H2O Al2O3粉末溶于NaOH溶液Al2O3+2OH-====2 +H2O
+H2O
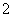 +H2O 铁溶于稀H2SO4∶Fe+2H+===Fe2++H2↑ Al(OH)3溶于NaOH溶液: Al(OH)3+3OH-===AlO
+H2O 铁溶于稀H2SO4∶Fe+2H+===Fe2++H2↑ Al(OH)3溶于NaOH溶液: Al(OH)3+3OH-===AlO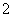 +3H2O
+3H2O