
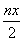 mol 反应中发生转移的电子数为3nx mol 在FeO·FeyCrxO3中3x=y 消耗硫酸亚铁铵的物质的量为n(2x+1)mol[
mol 反应中发生转移的电子数为3nx mol 在FeO·FeyCrxO3中3x=y 消耗硫酸亚铁铵的物质的量为n(2x+1)mol[
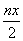 mol 反应中发生转移的电子数为3nx mol 在FeO·FeyCrxO3中3x=y
mol 反应中发生转移的电子数为3nx mol 在FeO·FeyCrxO3中3x=y
 mol 消耗硫酸亚铁铵的物质的量为n(2—x)mol
mol 消耗硫酸亚铁铵的物质的量为n(2—x)mol
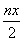 mol 反应中发生转移的电子数为3nx mol 在FeO·FeyCrxO3中3x=y
mol 反应中发生转移的电子数为3nx mol 在FeO·FeyCrxO3中3x=y
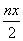 mo1 反应中发生转移的电子的物质的量为6nx mol 在FeO·FeyCrxO3中3x=y
mo1 反应中发生转移的电子的物质的量为6nx mol 在FeO·FeyCrxO3中3x=y