
 C分别在三种不同实验条件下进行,它们的起始浓度均为cA.=0.100 mol·L-1,c =0.200 mol·L-1, c =0 mol·L-1。反应物A. 的浓度随时间的变化如右图所示。下列说法正确的是
C分别在三种不同实验条件下进行,它们的起始浓度均为cA.=0.100 mol·L-1,c =0.200 mol·L-1, c =0 mol·L-1。反应物A. 的浓度随时间的变化如右图所示。下列说法正确的是  |
 C的△H.>0 C.实验②平衡时B.的转化率为60% 减小反应③的压强,可以使平衡时cA.=0.060 mol·L-1
C的△H.>0 C.实验②平衡时B.的转化率为60% 减小反应③的压强,可以使平衡时cA.=0.060 mol·L-1
 C的
C的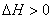 实验②平衡时B.的转化率为60% 实验③平衡时
实验②平衡时B.的转化率为60% 实验③平衡时
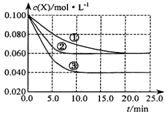
 C.(g)分别在三种不同实验条件下进行,它们的起始浓度均为cA.=0.100 mol·L.-1,c =0.200 mol·L.-1,c =0 mol·L-1。反应物A.的浓度随时间的变化如图所示。 下列说法正确的是 A.若反应①、②的平衡常数分别为K1、K2,则K1<K2 B.反应A.+2B
C.(g)分别在三种不同实验条件下进行,它们的起始浓度均为cA.=0.100 mol·L.-1,c =0.200 mol·L.-1,c =0 mol·L-1。反应物A.的浓度随时间的变化如图所示。 下列说法正确的是 A.若反应①、②的平衡常数分别为K1、K2,则K1<K2 B.反应A.+2B C的ΔH.>0 C.实验②平衡时B.的转化率为60% 减小反应③的压强,可以使平衡时cA.=0.060 mol·L.-1
C的ΔH.>0 C.实验②平衡时B.的转化率为60% 减小反应③的压强,可以使平衡时cA.=0.060 mol·L.-1 
 |