你可能感兴趣的试题
X.和R.在同一周期
原子半径:W.>R.>X
气态氢化物的稳定性:Y.>X
X.、Z.形成的化合物中只有离子键
Y.与Z.的原子序数之和可能为2a Y.的原子序数可能为a-17 Z.的原子序数可能为a+31 X.、Y.、Z.一定为短周期元素
Z.元素的原子半径可能比Y.元素的小 W.的原子序数可能是Y.的原子序数的2倍 W.的气态氢化物的稳定性一定比Y.的强 Z.的化学活泼性一定比X.强
Y、Z的原子序数之和可能是2a
Y的原子序数可能是a-17
Z的原子序数可能是a+31
X、Y、Z一定是短周期元素
随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 随着元素原子序数的递增,原子半径从小到大(稀有气体除外)发生周期性变化 元素性质的周期性变化是指原子核外电子排布原子半径及元素主要化合价的周期性变化
Z.元素的原子半径可能比Y.元素的小 W.的原子序数可能是Y.的原子序数的2倍 W.的气态氢化物的稳定性一定比Y.的强 Z.的化学活泼性一定比X.强 
图甲横坐标为原子序数,纵坐标表示元素的最高正价 图甲横坐标为核电荷数,纵坐标表示元素的原子半径(单位:pm) 图乙横坐标为最外层电子数,纵坐标表示元素的原子半径(单位:pm) 图乙横坐标为最高正价,纵坐标表示元素的原子半径(单位:pm)
同周期主族元素的原子序数越大越易失电子 同周期主族元素的原子序数越大半径越大z 同主族元素的原子序数越大非金属性越强 同主族元素的原子序数越大金属性越强
X.和R.在同一周期 原子半径:W.>R.>X. 气态氢化物的酸性:X.>Y. X.、Z.形成的化合物中阴阳离子个数比为1: 2
随着元素原子序数的递增,原子最外层电子数总是从1到8地重复出现 元素的性质随着原子序数的递增而呈周期性的变化 随着元素的原子序数的递增,元素的最高正价从+1到+7,负价从-7到-1地重复出现 元素性质的周期性变化是指原子核外电子排布的周期性变化、原子半径的周期性变化及元素主要化合价的周期性变化
W.的原子序数可能是Y.的原子序数的2倍 Z.元素的原子半径可能比Y.元素的小 W.的气态氢化物的稳定性一定比Y.的强 Z.的化学活泼性一定比X.强
元素性质随着核外电子周期性的排布而呈周期性的变化 同一周期的元素的第一电离能随着原子序数的递增,由小到大 同一周期的元素的原子半径随着原子序数的递增,由大到小 同一周期的元素的原子电负性随着原子序数的递增,由小到大 同一周期的元素的主要化合价随着原子序数的递增,由小到大
元素甲的简单气态氢化物稳定性比乙的强 元素乙在周期表中的位置为第二周期,ⅥA.族 4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 元素丙和元素丁的最高价氧化物对应的水化物均为强酸
W.的原子序数可能是Y.的原子序数的2倍
Z.元素的原子半径可能比Y.元素的小 W.的气态氢化物的稳定性一定比Y.的强
若Z.的最高正价为+m, 则X.的最高正价也一定为+m 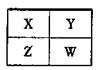
图甲可能表示的是元素单质的熔点随原子序数的变化关系 图甲可能表示的是元素原子的第一电离能随原子序数的变化关系 图乙可能表示的是元素原子的半径随原子序数的变化关系 图乙不可能表示同族元素的电负性随原子序数的变化关系
图甲横坐标为原子序数,纵坐标表示元素的最高正价 图甲横坐标为核电荷数,纵坐标表示元素的原子半径(单位:pm) 图乙横坐标为最高正价,纵坐标表示元素的原子半径(单位:pm) 图乙横坐标为最外层电子数,纵坐标表示元素的原子半径(单位:pm)
Y.的原子序数可能为a-17 Y.与Z.的原子序数之和可能为2a Z.的原子序数可能为a+31 X.、Y.、Z.一定为短周期元素
原子半径:Z>Y>X 气态氢化物的稳定性:R从Y.到R.对应的离子,Y.离子半径最小 Y.和Z.两者最高价氧化物对应的水化物能相互反应



